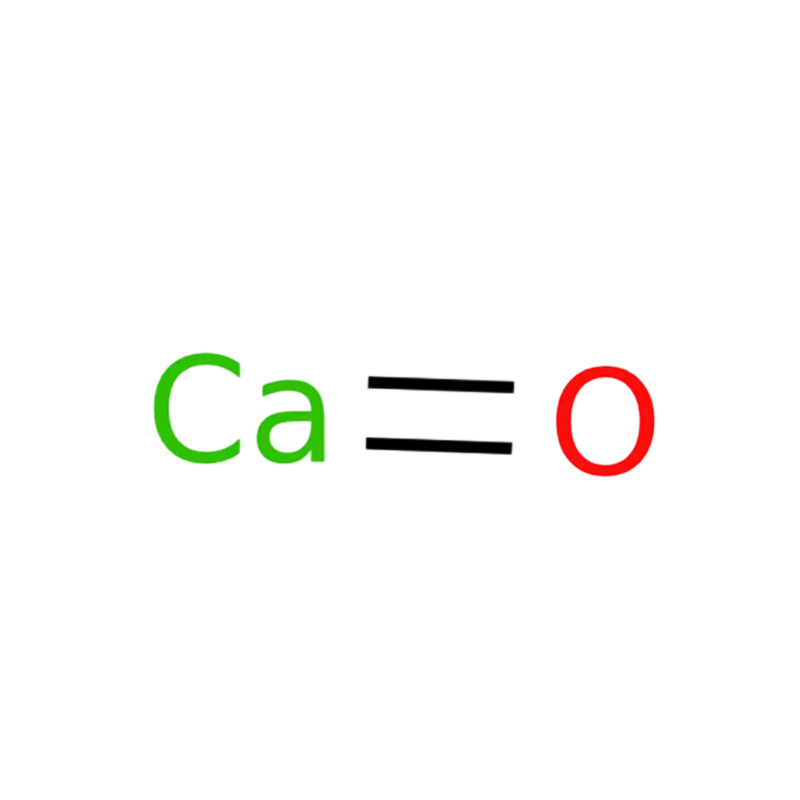Détails du produit
L'oxyde de calcium (CaO, n° CAS 1305-78-8), également appelé chaux vive ou calx, n'existe pas à l'état naturel car il réagit facilement avec l'eau pour former de la chaux hydratée et avec le dioxyde de carbone pour former du calcaire. Il est produit par calcination de matières premières carbonatées calciques telles que le calcaire ou les coquilles d'huîtres à une température de 1 700 à 2 450 °C.

Propriétés chimiques de l'oxyde de calcium
Point de fusion | 2570 °C |
Point d'ébullition | 2850 °C (litt.) |
Densité | 3,3 g/mL à 25 °C (litt.) |
Densité apparente | 800-1200 kg/m³ |
Indice de réfraction | 1.83 |
Fp | 2850°C |
Température de stockage | aucune restriction |
Solubilité | 1,65 g/l Risque de réaction violente |
Formulaire | poudre |
Couleur | Blanc à jaune très légèrement beige |
Gravité spécifique | 3.3 |
PH | 12,6 (H2O, 20℃)(solution saturée) |
Odeur | cristaux ou poudre blancs ou gris, inodores |
Solubilité dans l'eau | RÉAGIT |
Sensible | Sensible à l'air et à l'humidité |
Structure cristalline | Cubique |
Système de cristal | Cube |
Merck | 141 686 |
Groupe spatial | Fm3m |
Constante de réseau | a/nmb/nmc/nmα/oβ/oγ/oV/nm30.47760.47760.47769090900.1089 |
Constante diélectrique | 2.2 (Ambiant) |
Limites d'exposition | ACGIH : VME 2 mg/m3 |
OSHA : VME 5 mg/m3 | |
NIOSH : IDLH 25 mg/m3 ; VME 2 mg/m3 | |
Stabilité | Stabilité : Stable, mais absorbe le dioxyde de carbone de l’air. Incompatible avec l’eau, l’humidité, le fluor et les acides forts. |
InChIKey | ODINCKMPIJJUCX-UHFFFAOYSA-N |
Référence de la base de données CAS | 1305-78-8 (Référence de la base de données CAS) |
Référence de chimie du NIST | Monoxyde de calcium (1305-78-8) |
Système d'enregistrement des substances de l'EPA | Oxyde de calcium (1305-78-8) |
Application
La chaux trouve de nombreuses applications dans divers secteurs industriels, notamment la métallurgie, la désulfuration des gaz de combustion, la construction, l'exploitation minière, la papeterie et le traitement de l'eau. Dans la purification du minerai de fer, l'oxyde de calcium joue un rôle essentiel dans l'élimination des impuretés par réaction avec des composés tels que les silicates, les phosphates et les sulfates présents dans le minerai, formant ainsi du laitier.

Emballage et expédition